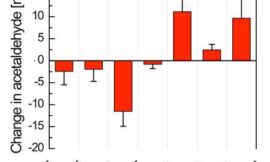
El potencial de oxidorreducción, o potencial redox, designado como EH, es una medida muy antigua; los primeros trabajos sobre vinos son los de Gélosos y datan de 1931. Jean Ribéreau-Gayon contribuyó, a su vez, a la adquisición de estos conocimientos; a él se debe una obra de referencia sobre los diversos aspectos de las oxidaciones y reducciones de los vinos, en 1933. Es a partir de estas dos contribuciones determinantes que pudo escribirse, más tarde, 70 años de ciencias y técnicas de oxidorreducción de los vinos. Siguiendo el mismo planteamiento que Jean Ribéreau-Gayon, hemos descubierto una síntesis más reciente del mismo. La oxidorreducción, medida por el potencial del mismo nombre, con la ayuda del electrodo polarigráfico específico, es un dato que siempre es delicado de interpretar y ha sido integrado en la práctica de las bodegas. El potencial de oxidorreducción, EH, que se mide en mV, representa una fotografía instantánea del estado de oxidación o de reducción de una solución; al igual que el pH, que expresa el estado ácido-básico de un vino en un instante «t». El EH se mide con la ayuda de electrodos, del mismo modo que el pH, y da resultados cualitativos. Sin embargo, como sucede con el pH, el único valor de EH es insuficiente, se necesita, pues, una medida complementaria de naturaleza cuantitativa: la acidez total para el pH y el contenido en oxígeno disuelto para el EH.
El interés creciente por el concepto de oxidorreducción en los vinos tiene sus raíces en las dos grandes revoluciones enológicas. Al inicio de nuestra historia vinícola, el arte y la forma de elaborar el vino pretendían únicamente producir una bebida alcohólica coloreada, franca de gusto y olor; el vino consumido durante el año no debía oxigenarse, la enología era reductora. Después de la primera revolución enológica iniciada por Pasteur, se impuso una enología curativa, que pretendía prevenir las contaminaciones microbianas. Desde entonces se podía utilizar oxígeno sin reserva, tanto más fácilmente después de lo que Pasteur decía, «el oxígeno es el que hace el vino; es debido a él por lo que envejece»; se estaba desarrollando una enología oxidativa. Pero los olores se desvanecían, se oxidaban y la pérdida rápida del color de los vinos tintos o el oscurecimiento de los vinos blancos mostraron los límites de una práctica aplicada con rigurosidad.
Durante la segunda revolución enológica, iniciada por Ribéreau-Gayon y reanudada por la escuela Bordelesa que él había creado, se desarrolló una enología preventiva permitida por la generalización del empleo de antisépticos y antioxidantes (SO2, ácido ascórbico, ácido sórbico, …), reglas de higiene y la llegada de una microbiología del vino. Es en este mismo período que la noción de oxidación bien empleada avanzó. Se puede definir esta tercera enología, como enología de compromiso, en la cual se utiliza de forma razonada la reducción y la oxidación. El desarrollo de las técnicas de hiperoxigenación, de remontado de cubas de fermentación con aire o con azufre, de conservación mediante gas inerte, de efervescencias o de microoxigenación en cuba de conservación, de trasiego controlado de los vinos en barricas, de embotellado con gas neutro, son algunas de las pruebas. Para cualquiera de estas tecnologías, la medida del potencial redox es primordial para controlar el efecto del tratamiento y las condiciones de su aplicación sobre el estado del vino. Incluso hoy, aún la generalización de esta medida está pendiente, y su asimilación mediante los análisis enológicos rutinarios requiere un largo recorrido de aprendizaje.
Medida, variación y significación del EH en los vinos
El EH se mide en el mosto o el vino sumergiendo en el medio, un electrodo o un sistema de electrodos específicos (Vivas et al., 1996). El valor del EH, siendo extremadamente sensible y sujeto a variación, es preferible medirlo directamente en el medio circundante del vino sin tener que recurrir a métodos más o menos complejos de extracción de muestra. El valor del EH se rige por la ley de Nerts, que resume esencialmente los factores susceptibles de hacerlo variar. Ésta viene definida por:
EH (mV) = E0 – ApH + BLog[O2]
El EH depende, pues, de los pares redox del vino, esencialmente se trata de los polifenoles, evaluados por la relación entre el contenido en forma oxidada (Ox) y reducida (Rd), para cada par redox (E0). El E0 corresponde al potencial normal para el cual tenemos exactamente el 50 % de cada una de las dos formas [(Ox)/(Rd) = 1]. Esta magnitud es característica de un par redox. En el caso particular del vino, la suma de los pares redox, E0, se comporta como un conjunto homogéneo (Vivas, 1999), presentando un potencial normal denominado E0v, o potencial normal del vino (Vivas et al., 1992 ; Vivas et al., 1999). El valor del EH depende del pH y del contenido en oxígeno disuelto. A y B son los coeficientes de dependencia del EH para estos dos últimos parámetros. Así el incremento del pH provoca la disminución del E; e inversamente, el incremento del contenido de oxígeno disuelto es responsable del aumento del E.
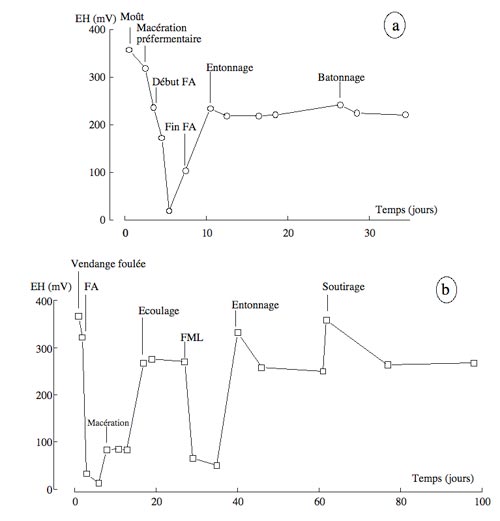
Un ejemplo práctico de la evolución de los valores del EH, durante la vinificación y elaboración de los vinos tintos y blancos puede verse en la figura 1. En ella puede observarse que los mostos, siempre más oxidables que los vinos correspondientes, tienen potenciales redox elevados, superiores a 350 mV. Posteriormente, las fermentaciones alcohólica y maloláctica (en tintos) hacen disminuir el EH (< 100 mV), incluso a veces hasta valores negativos (- 50 mV). Finalmente, en los vinos ya terminados, las variaciones del EH son mucho menos importantes, puesto que los valores varían entre 150 y 250 mV. En promedio, el EH es más elevado en barricas que en cubas, a parte de los períodos específicos de oxidaciones. Solamente la presencia de lías o aireaciones considerables provocan saltos del EH (en la mayor parte de los casos de ± 50 a 75 mV). De hecho, la medida regular del EH proporciona informaciones sobre las tendencias de la evolución del vino. Por ejemplo, si el EH medio tiende a disminuir, se puede esperar la aparición de caracteres de reducción fáciles de prevenir mediante un ligero trasiego, o simplemente mediante un aporte de oxígeno con los dispositivos adecuados. Y a la inversa, si el EH aumenta bruscamente debido a un trasvase de cuba, o un tratamiento de microoxigenación, se pueden limitar estos efectos en el vino, bien sea corrigiendo el modo de intervención para hacerlo menos oxidante, o bien añadiendo a las lías frescas levaduras o derivados de levaduras industriales con efectos reductores.
Estimación del equilibrio redox del vino mediante el cálculo del potencial normal del vino EOV
La medida se basa en la diferencia de superficie entre una curva teórica, obtenida por cálculo, que es característica de cada vino, y los resultados experimentales del EH obtenidos durante les 96 horas siguientes a la saturación en oxígeno del vino. La aproximación teórica del potencial redox conduce a dos expresiones del EH: la ecuación simple de Nerst, que ya hemos visto anteriormente y la ley general de Nerst, por la cual el EH viene en función del potencial normal del medio (E0), así como del logaritmo neperiano de la razón entre la concentración de sustancias oxidadas y reducidas:
EH (mV) = E0 + (RT/nF) Ln([Ox]/[Red])
Estas dos ecuaciones complementarias no evolucionan en el mismo sentido. Después de la primera ecuación, después de la oxigenación del vino, se observa una disminución del factor [O2], luego el EH debe disminuir. En cambio, después de la segunda ecuación, después de una oxidación, el contenido en compuestos oxidados aumenta, mientras que el contenido en compuestos reducidos disminuye, lo que provoca un aumento del EH. Cuando se determina, para cada vino, la primera ecuación, el tiempo muy corto de medida (alrededor de 10 min), no permite observar variación sensible alguna de la fracción ([Ox]/[Red]). Pero cuando se estudian las variaciones del EH con el tiempo, después de una oxigenación, esta ecuación ya no es suficiente. Para responder a esta doble exigencia, proponemos una expresión sintética del EH, teniendo en cuenta las ecuaciones de ambas:
EH’ = E0 + (RT / nF) Ln([Ox]/[Red]) – ApH + BLog[O2]
Se puede escribir Eov = Eo+ (RT / nF) Ln([Ox]/[Red]), que representa el estado de oxidación del vino. Hemos demostrado, por otra parte, que el valor de A es, en los vinos, constante e idéntico al obtenido mediante cálculo. A es aproximadamente igual a 59,15. La expresión puede escribirse como:
EH = E0 = Eov – 59,15pH + BLog [O2]
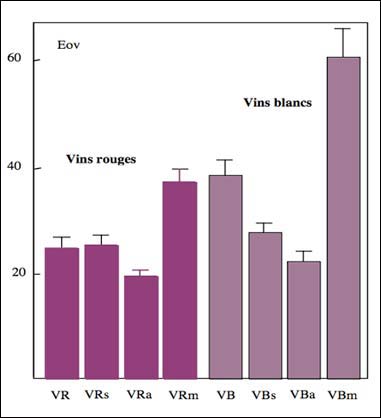
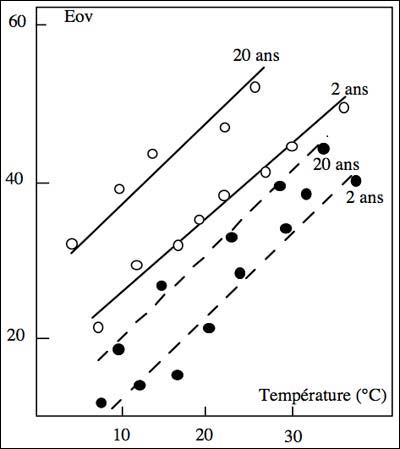
He aquí algunas aplicaciones prácticas del enfoque. En la figura 2 se hallan representados los resultados de una experiencia realizada sobre un vino tinto y uno blanco. Hemos estudiado el papel del SO2, del ácido ascórbico, del hierro y del cobre, del que se conocen los efectos sobre las reacciones de oxidorreducción de los vinos (Vivas et al., 1992; Vivas et al., 1997). Se muestra que el SO2 presenta un verdadero efecto antioxidante sobre los vinos blancos, contrariamente a los vinos tintos, para los cuales no parece tener efecto medible. Este resultado está en consonancia con nuestros trabajos anteriores sobre el mismo (Vivas et al., 1993; Vivas y Glories 1996; Vivas et al., 1997). El ácido ascórbico es un antioxidante con una actividad instantánea tanto en los vinos tintos como blancos. Los metales de transición testados (Fe II y Cu I) aumentan netamente el estado de oxidación de los vinos. Así los vinos son más sensibles al oxígeno. En otra serie de análisis, los vinos de 20 años están más oxidados que los vinos jóvenes de dos años (fig. 3). Estos resultados son sorprendentes en cuanto que se considera, generalmente, que en la botella los vinos se reducen. Por otra parte, el incremento de la temperatura aumenta sensiblemente su oxidabilidad; provocando la moderación termodinámica de las velocidades de oxidación y de reducción. Estos primeros resultados indican la intervención del calor y de la conservación en botellas en la evolución de los vinos hacia un estado de oxidación superior al del nivel inicial.
La valoración potenciométrica: otra medida del potencial redox que permite prever la evolución oxidativa de los vinos
La valoración potenciométrica es un método global de medida del conjunto de pares redox de un vino (Vivas et al., 2008). El método permite evaluar y seguir la evolución de la sensibilidad del vino a la oxidación en el transcurso del tiempo y en función de las operaciones y procesos súbitos. Durante la crianza, los vinos, bajo el efecto de fenómenos oxidativos, ganan en estabilidad, lo que se traduce en un aumento de su resistencia al oxígeno. Se trata de la evolución normal de los vinos. El caso contario, es decir, el incremento de la sensibilidad de los vinos al oxígeno, se considera cuando la crianza es demasiado oxidante, o demasiado brusca, o bien que el vino es particularmente sensible. En la figura 4, hemos reagrupado las curvas de valoración potenciométrica de un vino merlot negro en cuya crianza en barricas utiliza tres tipos de estructuras distintas de madera. Todas las muestras evolucionan correctamente y es interesante constatar que cuanto más compacta es la estructura, es más poroso el vino (Vivas et al., 2003), y más resistente a la oxidación al final de su crianza. Ello representa la primera demostración de la relación entre la estructura de la madera y la intensidad de los fenómenos oxidativos. Si, al final de la crianza, clasificamos los vinos en función de la resistencia creciente a la oxidación, obtenemos la siguiente relación: texturas gruesas < texturas medias < texturas compactas. En la tabla 1 hemos agrupado los valores de las experiencias de valoración potenciométrica para el ensayo considerado. Puede verse que en el curso del tiempo, la variación del porcentaje de oxidante necesario para la valoración completa de cada muestra es tanto más débil cuanto más porosa es la madera. Ello se comprueba en las muestras de octubre y febrero. Los mayores desvíos se registran con texturas apretadas y toscas, los dos extremos del experimento.
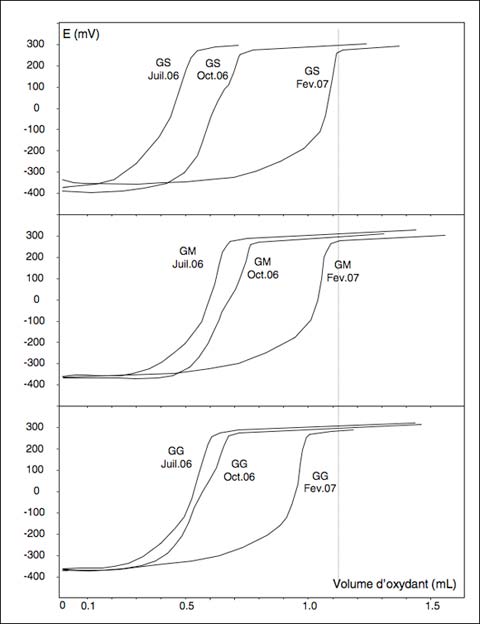
GS) textura compacta. GM) textura media. GT) textura tosca.
Valoración en oxidación por DCPIP N/20, 0,02 mL/30 s, muestra diluida al 1/50 en solución hidroalcohólica
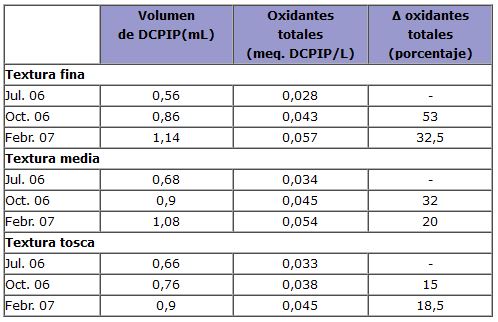
Conclusiones
Los trabajos sobre la oxidorreducción de los vinos, han obtenido en estos últimos veinte años un desarrollo importante, en particular con las herramientas utilizadas frecuentemente. En principio la medida directa del EH en los vinos proporciona una imagen, en un instante determinado, del estado redox. El cálculo del E0V, o potencial normal del vino, es una expresión de equilibrio entre las formas reducidas y oxidadas. Finalmente la valoración potenciométrica representa la medida, en función del tiempo, de la oxidabilidad del vino o su sensibilidad al oxígeno. Estas diferentes aproximaciones analíticas permiten controlar el vino a través de las diferentes operaciones de trabajo y tratamiento.
Bibliografía
Géloso, J. Relation entre vieillissement des vins et leur potentiel d’oxydoréduction. Ann Brass Distil 1931; 29: 193-273.
Ribéreau-Gayon, J. Contribution à l’étude des oxydations et des réductions dans les vins. Application à l’étude du vieillissement et des casses. Delmas (Ed.), Burdeos, 1993, 126 p.
Vivas N., Zamoro F. y Glories Y. Etude des phénomènes d’oxydoréduction dans les vins. Mise au point d’une méthode rapide de mesure du potentiel d’oxydoréduction. J Int Sc Vigne Vin 1992; 26: 4: 271-285.
Vivas, N., Zamora, F. y Glories, Y. Incidence de certains facteurs sur la consommation de l’oxygéne et sur le potentiel d’oxydoréduction dans les vins. J Int Sc Vigne Vin 1993; 27: 23-34.
Vivas, N., Glories, Y. , Bertrand, A. y Zamora, F. Principe et méthode de mesure du potentiel d’oxydoréduction dans les vins. Bull OIV 1996; 69: 617-633.
Vivas, N., Saint-Cricq de Gaulejac, N. y Glories, Y. Influence de SO2 et de l’acide ascorbique sur l’activité antiradicalaire des tanins, mesurée sur l’anion superoxyde. Application aux vins rouges. Vitis, 1997, 36: 91-96.
Vivas, N., Saint-Cricq de Gaulejac, N. y Zamora, F. Experimental principle to evaluate the degree of oxidation or reduction balance in wines. J Sci Tech Tonnellerie 1999; 5: 71-76.
Vivas, N., Debeda, H., Menil, N., Vivas de Gaulejac, N. y Nonier, M.F. Mise en évidence du passage de l’oxygène au travers des douelles constituant les barriques par l’utilisation d’un dispositif original de mesure de la porosité du bois. Premiers résultats. Sci Aliments 2003; 23: 655-768.
Vivas, N., Vivas de Gaulejac, N. y Nonier, M.F. Une méthode usuelle pour l’estimation de l’oxydabilité des vins. Bull OIV 2008; 929-931: 357-379.
Vivas, N. y Glories, Y. Effet antioxydant de l’anhydride sulfureux dans les vins rouges. Riv Vitic Enol 1996; XLIX: 51-56.
Vivas, N. Les oxydations et les réductions dans les moûts et les vins. Féret (Ed.), Bordeaux, 1999, 164 p.